Dendrites dans les batteries lithium : causes et conséquences

Les dendrites sont de petites aiguilles de lithium métal qui se forment à l’intérieur des cellules quand le dépôt de lithium n’est pas uniforme. On ne les voit pas, mais elles peuvent dégrader une cellule très vite et mettre en péril un pack complet. Le phénomène apparaît surtout quand on cherche beaucoup de densité énergétique et de puissance de charge.
Comment elles apparaissent
Quand on recharge, les ions lithium quittent la cathode et se déposent sur l’anode. Idéalement, le dépôt est homogène. En pratique, il suffit d’une densité de courant trop élevée, d’une température trop basse, d’une surface d’anode irrégulière ou d’une couche SEI instable pour que le lithium commence à se déposer par endroits. Ces points de croissance s’allongent cycle après cycle et donnent des dendrites.
Plusieurs paramètres favorisent la formation de dendrites, souvent liés aux conditions de charge et à la conception interne de la cellule :
- Charge trop rapide (au-delà de 1C) : un courant élevé pousse les ions lithium à se déposer plus vite qu’ils ne peuvent se répartir uniformément sur l’anode. Cela crée des zones de concentration où les dendrites commencent à croître. La valeur "1C" correspond à une recharge complète en une heure. Par exemple, une batterie de 60 kWh rechargée à 60 kW est chargée à 1C. À 120 kW, on atteint 2C. Plus le courant dépasse cette valeur, plus le risque de dépôt irrégulier augmente.
- Répartition inégale du courant dans l’électrolyte : un flux d’ions mal dirigé, dû à une géométrie interne imparfaite ou à une faible conductivité de l’électrolyte, provoque des dépôts localisés au lieu d’un film homogène de lithium.
- Pression interne insuffisante : dans une cellule lithium métal, une légère compression mécanique maintient le contact entre électrolyte et électrode. Si cette pression est trop faible, le dépôt devient irrégulier et favorise la croissance verticale des dendrites.
- Couche SEI instable : la couche protectrice qui se forme sur l’anode se fissure à chaque cycle à cause des variations de volume. Ces microfissures exposent des zones réactives où le lithium se redépose de manière anarchique, ce qui déclenche de nouveaux points de croissance.
Rôle et fragilité de la couche SEI
La SEI (Solid Electrolyte Interphase) est une fine couche protectrice qui se forme naturellement à la surface de l’anode dès les premiers cycles. Elle résulte d’une réaction entre l’électrolyte et le lithium. Son rôle est essentiel : elle isole électriquement le lithium tout en laissant passer les ions. Sans elle, le lithium réagirait directement avec l’électrolyte et la cellule se dégraderait très vite.
Mais cette couche est instable. Elle se fissure quand le volume de l’anode change pendant les cycles de charge et de décharge. À chaque fissure, une nouvelle SEI se reforme par réaction chimique, consommant encore du lithium et de l’électrolyte. Cela provoque une perte progressive de capacité et rend le dépôt de lithium irrégulier, ce qui favorise la croissance des dendrites. Une SEI trop épaisse augmente aussi la résistance interne, ce qui échauffe davantage la cellule et accentue encore le problème.
Conséquences
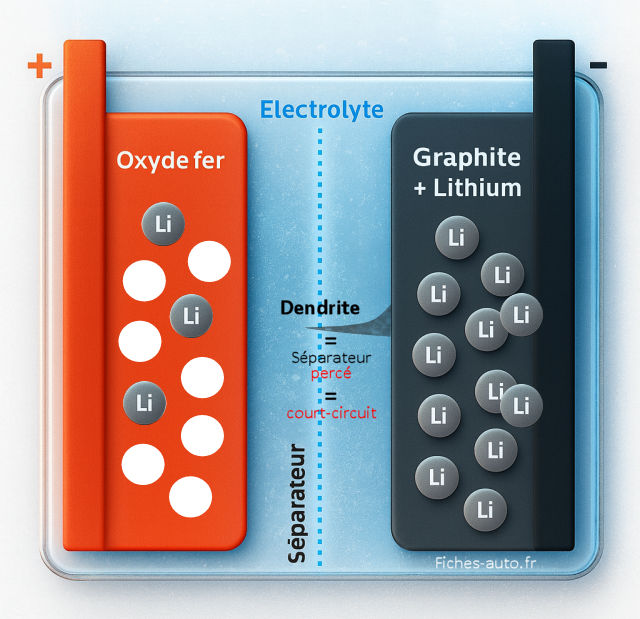
Séparateur percé
Première étape, on perd de la capacité utile. Du lithium se retrouve piégé dans les dendrites au lieu de participer à la réaction. La résistance interne augmente, la chauffe aussi.
Étape suivante, les dendrites grandissent et finissent par toucher le séparateur. Si elles le percent, on a un court-circuit interne entre anode et cathode. La température grimpe, l’électrolyte peut dégazer et l’emballement thermique devient possible. Ce n’est pas seulement une baisse de performance, c’est un vrai sujet de sécurité.
La progression d’une dendrite à travers le séparateur dépend surtout de la résistance mécanique de ce dernier. Les séparateurs en polyéthylène ou polypropylène ont une épaisseur typique de 15 à 25 microns, avec des pores d’environ 0,05 µm. Dès que la pointe métallique atteint ces pores, elle peut les traverser si le différentiel de potentiel est suffisant. Certains fabricants testent désormais des séparateurs céramiques ou des couches doubles renforcées pour limiter cette perforation, mais cela alourdit la cellule et réduit légèrement sa densité énergétique.
Couche SEI
Même sans court-circuit, la dégradation accélère : SEI qui s’épaissit, chute du rendement coulombique, perte de capacité en quelques dizaines à centaines de cycles selon les cas.
La couche SEI se comporte un peu comme une peau cicatrisante sur l’anode. À chaque cycle, elle se fissure et se reforme, en consommant du lithium actif. Plus elle s’épaissit, plus elle devient résistive, ce qui dégrade le rendement coulombique. Une SEI stable garde un bon équilibre entre perméabilité ionique et isolation électronique, mais si elle devient poreuse ou hétérogène, le lithium commence à se déposer en dehors de sa zone prévue. C’est souvent à partir de ces irrégularités que les premières dendrites apparaissent. Une SEI mal contrôlée peut réduire la durée de vie d’une cellule de moitié, voire plus sur les chimies à lithium métal.
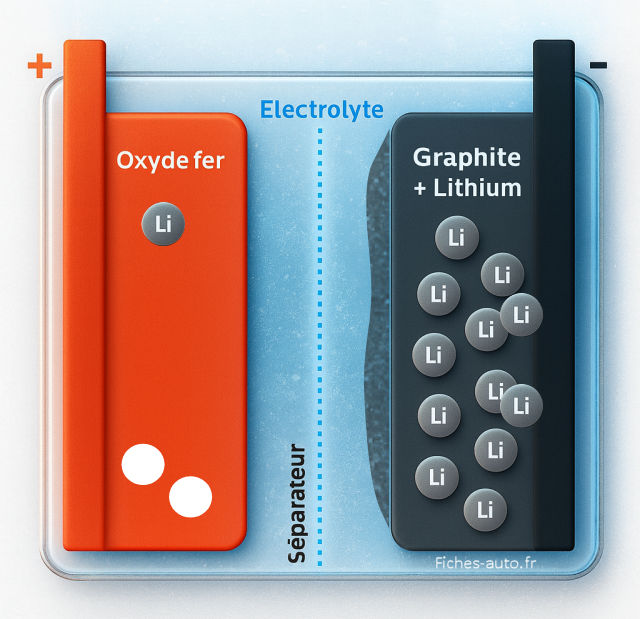
Batteries sans anode et sensibilité accrue
Dans une cellule dite sans anode, on ne fabrique pas d’anode graphite. On ne garde qu’un collecteur en cuivre côté négatif et l’anode se forme lors de la première charge par dépôt de lithium métal. C’est efficace sur le papier, mais très délicat à maîtriser. Le moindre défaut d’homogénéité au dépôt favorise les dendrites.
Ordres de grandeur observés en conditions de labo :
- Densité énergétique possible de 350 à 500 Wh/kg
- Durée de vie souvent limitée à 150 à 200 cycles complets, meilleurs cas autour de 400 cycles avec protocoles très contrôlés
- Dépôt plus régulier entre 25 et 45 °C, électrolytes additivés requis
- Charge agressive au-delà de 1 à 2 C qui augmente clairement le risque
Comment limiter le phénomène
- Travailler l’électrolyte et ses additifs pour obtenir un dépôt plus uniforme
- Texturer ou enrober la surface du collecteur pour guider la nucléation du lithium
- Maintenir une pression interne suffisante dans la cellule
- Gérer la charge avec des profils adaptés : limitation du courant en fin de charge, températures contrôlées, coupures si échauffement anormal
- Sur les architectures solides ou semi-solides, utiliser des interfaces plus stables, même si d’autres contraintes apparaissent
Conclusion
Les dendrites sont le verrou récurrent des chimies à lithium métal et des variantes sans anode. Tant que le dépôt restera hétérogène, la sécurité et la longévité bloqueront l’industrialisation large. Les gains potentiels en densité énergétique sont réels, mais ils ne tiennent que si l’on garde un dépôt propre et stable au fil des cycles. Pour l’instant, c’est jouable en labo avec des protocoles stricts. En usage automobile, il reste du chemin.
Ces articles pourraient vous intéresser :
- Comment une batterie lithium peut prendre feu ?
- Le vieillissement et la dégradation des batteries au lithium
- A quelle vitesse se dégradent les batteries de voiture électrique ?
- Bonnes habitudes pour réduire la dégradation de la batterie
Ecrire un commentaire
Sondage au hasard :
Trouvez-vous les montants des PV bien adaptés aux infractions commises ?
© CopyRights Fiches-auto.fr 2026. Tous droits de reproductions réservés.
Nous contacter - Mentions légales
Fiches-auto.fr participe et est conforme à l'ensemble des Spécifications et Politiques du Transparency & Consent Framework de l'IAB Europe. Il utilise la Consent Management Platform n°92.
Vous pouvez modifier vos choix à tout moment en cliquant ici.




